Existem três tipos fundamentais de misturas: as homogêneas (homo: igual), as heterogêneas (hetero: diferente) e as coloidais.
Misturas heterogêneas
Uma mistura é dita heterogénea quando apresenta duas ou mais fases e os componentes da mistura são perceptíveis. Observação: a visualização não é, necessariamente, a olho nu. As fases de uma mistura heterogênea podem ser detectadas no microscópio ou separadas em uma centrífuga. Como exemplos têm-se o sangue e o leite.Mistura homogênea
A mistura homogênea é aquela cujas substâncias constituintes não podem ser identificadas, pois possuem as mesmas propriedades em toda a sua extensão. Tais substâncias sofrem dissolução, ou seja, a sua mistura produz somente uma fase. Isso quer dizer que toda mistura homogênea é uma solução, ou seja, mistura homogênea é um conjunto de substâncias solúveis entre si. Um exemplo é a mistura da água com álcool: quando misturadas essas duas substâncias é impossível distinguir uma da outra.Outro exemplo é a mistura de água e sal de cozinha, seguindo o mesmo padrão da mistura anterior.Misturas coloidais: Nas misturas coloidais, os componentes da mistura não se distinguem a olho nu, contudo se usarmos um instrumento de ampliação, como um microscópio, é possível distinguir os diferentes componentes da mistura.
Por exemplo, se observares uma gota de sangue a olho nu não consegues identificar os seus componentes, mas se observares essa gota ao microscópio, distingues os glóbulos brancos, os glóbulos vermelhos, as plaquetas, etc.
Gases formam misturas homogêneas exceto quando suas densidades são muito diferentes, como o hexafluoreto de urânio (UF6) com hélio (He).
Misturas Azeotrópicas e Eutéticas
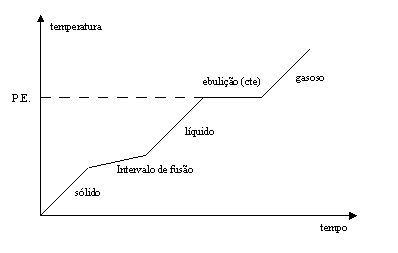
Algumas misturas apresentam características iguais às de elementos ou compostos químicos na hora da ebulição ou de fusão.- Misturas Azeotrópicas: são misturas em que o ponto de ebulição não se altera, em temperatura constante, comportando-se como um composto químico ou um elemento. Esse tipo de mistura acontece quando o ponto de ebulição atinge o patamar.É muito comum entre líquidos. Ex.: O álcool hidratado é uma mistura azeotrópica, isso se deve porque esse álcool está misturado à água em uma proporção onde é impossível separar pela ebulição, já que a temperatura se mantém constante. PE = 78,5°C; PF = -177°C; P = 0,79g/cm³ são os pontos de fusão (PF) e ebulição (PE) do álcool.
- Misturas Eutéticas: são misturas em que o ponto de fusão dos elementos que a compõem são maiores que o da mistura eutética. Isso é muito comum em misturas entre metais. Ex.: o bronze é uma mistura de cobre com o estanho, impossível separar por fusão.
Separação de misturas
As misturas podem ser separadas usando os seguintes métodos:- Decantação: permite a separação de líquidos imiscíveis (que não se misturam) ou um sólido precipitado num líquido. Exs.: água e areia, água e óleo vegetal. Pode-se aproveitar a pressão atmosférica e a gravidade para auxiliar no processo de decantação. Um dos líquidos pode ser retirado por sifonação, que é a transferência, através de uma mangueira, de um líquido em uma posição mais elevada para outra, num nível mais baixo.
- Filtração: este é um método de separação muito presente no laboratório químico e também no cotidiano. É usado para separar um sólido de um líquido ou sólido de um gás, mesmo que o sólido se apresente em suspensão. A mistura atravessa um filtro poroso, onde o material particulado fica retido.
- Centrifugação: para separar líquidos imiscíveis (que não se misturam) ou um líquido de um sólido insolúvel em suspensão. Para fazer uma centrifugação é preciso uma centrifugadora. Esta máquina faz rodar a mistura (na qual uma das partes tem que ser líquida) a alta velocidade, provocando a separação pela ação da força que é aplicada (do centro para fora). A separação dá-se devido às diferenças de densidades dos materiais. Normalmente uma centrifugação é seguida de uma decantação.Ex: separar glóbulos vermelhos do plasma sanguíneo; separar a nata do leite.
- Cristalização: separa um sólido cristalino de uma solução. Na cristalização há uma evaporação do solvente de uma solução provocando o aparecimento de cristais do soluto. Ex: o aparecimento do sal nas salinas.
- Destilação: separa líquido(s) de sólido(s) dissolvidos ou líquido(s) de líquido(s). Na destilação acontecem duas mudanças de estado consecutivas: uma ebulição (vaporização) seguida de uma condensação. Na ebulição é retirado da mistura o componente com o ponto de ebulição mais baixo, e na condensação esse componente volta à sua forma líquida. Existe um tipo de destilação, a destilação fracionada, que permite a separação de vários líquidos com pontos de ebulição muito próximos. Ex: obtenção de água destilada, aguardentes; separação dos diferentes componentes do petróleo.
- Destilação Fracionada: é um método de separação de líquidos que participem de mistura homogênea ou heterogênea. Quanto mais distantes forem os pontos de ebulição destes líquidos, mais eficiente será o processo de destilação. Eleva-se a temperatura até que se alcance o ponto de ebulição do líquido que apresente valor mais baixo para esta característica e aguarda-se, controlando a temperatura, a completa destilação deste. Posteriormente, permite-se que a temperatura se eleve até o ponto de ebulição do segundo líquido. Quanto mais próximos forem os pontos de ebulição dos líquidos, menor o grau de pureza das frações destiladas. A destilação fracionada é usada na obtenção das diversas frações do petróleo.
- Cromatografia: para separar substâncias com diferentes solubilidades num determinado soluto. Na cromatografia uma mistura é arrastada (por um solvente apropriado) num meio poroso e absorvente. Como diferentes substâncias têm diferentes velocidades de arrastamento num determinado solvente, ao fim de algum tempo há uma separação dos constituintes da mistura. Este processo é normalmente usado para pequenas quantidades de amostra. Ex: separação dos componentes de uma tinta.
- Separação Magnética: consegue separar componentes que tenham propriedades magnéticas dos que não as possuem. Aproveitam-se as propriedades magnéticas de um dos componentes da mistura para o separar dos outros. Ex: areia e limalha de ferro; enxofre e limalha de ferro.
- Extração por Solvente: para usar este processo usa-se um solvente que só dissolve um dos constituintes da mistura.Ex: extração da cafeína do chá, usando clorofórmio; remover o iodo da água de iodo, com clorofórmio.
- Catação: é um método de separação bastante rudimentar, usado para separação de sistemas sólido-sólido. Baseia-se na identificação visual dos componentes da mistura e na separação dos mesmos separando-os manualmente. É o método utilizado na limpeza do feijão antes do cozimento.
- Peneiração: também conhecido como tamisação, este método é usado na separação de sistemas sólido-sólido, onde um dos dois componentes apresente granulometria que permita que o mesmo fique preso nas malhas de uma peneira.
- Ventilação: método de separação para sistemas sólido-sólido, onde um dos componentes pode ser arrastado por uma corrente de ar. Um bom exemplo é a separação da casca e do caroço do amendoim torrado.
- Levigação: a água corrente arrasta o componente menos denso e o mais denso deposita-se no fundo do recipiente. Um bom exemplo é a lavagem da poeira do arroz ou até mesmo a separação do ouro, em garimpos.
- Fusão Fracionada: processo usado para separar sólidos cujos pontos de fusão são muito diferentes (Transformação do sólido para o líquido). Exemplo: Ouro e bronze, que tem a densidade diferente, ocasionando a fusão mais rápida do bronze.
- Solidificação Fracionada: Processo usado para separar líquidos cujo ponto de solidificação são muito diferentes.
- Flotação: técnica de separação muito usada na indústria de minerais, na remoção de tinta de papel e no tratamento de água, entre outras utilizações. A técnica utiliza diferenças nas propriedades superficiais de partículas diferentes para as separar. As partículas a ser flotadas são tornadas hidrofóbicas pela adição dos produtos químicos apropriados. Então, fazem-se passar bolhas de ar através da mistura e as partículas que se pretende recolher ligam-se ao ar e deslocam-se para a superfície, onde se acumulam sob a forma de espuma. Exemplo: Separar a serragem da areia, que usa a água para separá-los; fazendo a serragem ficar na superfície e a areia no fundo do pote.
Nenhum comentário:
Postar um comentário