Unidade de massa atômica (uma)
A unidade de massa atômica, ou dalton é uma unidade de medida de massa utilizada para expressar a massa de partículas atômicas (massas atômicas de elementos ou compostos). Ela é definida como 1/12 da massa de um átomo de carbono-12 em seu estado fundamental [1].Seu símbolo é u, uma ou Da, e a seguinte equivalência é válida (CODATA, 2007)[2]:
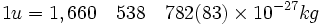 Não é uma unidade do Sistema Internacional de Unidades, mas é aceita por este.
Não é uma unidade do Sistema Internacional de Unidades, mas é aceita por este.Obs.: O 12C foi escolhido em 1962 e é usado atualmente em todos os países do mundo.
Massa atômica
Massa atômica ou número de massa (representada pela letra A) é a soma do peso dos prótons e neutrons do núcleo de um átomo, peso medido em unidade de massa atómica, representado por u.Pela definição de u (unidade de massa atômica), sabe-se que u corresponde a 1/12 da massa do Carbono-12. Como a massa atômica é expressa em u, ela indica quantas vezes a massa de um átomo é maior que 1/12 da massa de Carbono-12.
Por exemplo referir que a massa atômica de um dado isótopo do Flúor é 19 u, indica que o isótopo em questão é 19 vezes "mais pesado" que 1/12 da massa do Carbono-12.
Atualmente o termo peso atômico deve ser evitado, por ser incorreto.
Massa atômica de um elemento químico
O cálculo da massa atómica de um elemento químico, também referida como a massa atômica relativa, é feito matemáticamente tendo em conta a frequência relativa dos isótopos do elemento.Por exemplo há dois isótopos conhecidos do Cloro, sendo eles o Cloro-35 e o Cloro-37. O primeiro, com massa atômica de 34,9689 u tem uma ocorrência na natureza em torno de 75,77%, enquanto que o outro isótopo, de massa 36,96590 u, tem uma ocorrência de 24,23%. Dito de outra forma, qualquer amostra de átomos de Cloro será constituida por sensivelmente 75,77% de átomos de Cloro-35 e 24,23% de átomos de Cloro-37.


Onde Ma é a massa atômica do elemento químico.
Conforme exposto acima, levando em consideração a ocorrência na natureza, sabe-se que a massa atômica do elemento Cloro é de 35,45 u.
Massa atômica de uma substância
Uma definição semelhante aplica-se às moléculas - sendo então chamada massa molecular de uma substância, expressa em u.A massa da molécula de uma dada substância é calculada pela soma das massas atômicas de todos os seus átomos constituintes. Esta técnica deixa de lado apenas a energia de ligação química, que geralmente é negligível.
Ex.: A molécula de metano é composta por 1 átomo de carbono e 4 átomos de hidrogênio. Sabendo que a massa atômica do hidrogênio é aproximadamente 1 u e a do carbono aproximadamente 12 u, então a massa atômica da substância metano (massa de uma molécula de metano) é calculada da seguinte forma:

Nenhum comentário:
Postar um comentário